Les techniques de stimulation cérébrale non invasive (NIBS) sont aujourd’hui des outils indispensables dans la recherche et l’application cliniques. Elles offrent des moyens innovants permettant d’agir de manière ciblée et douce sur des zones spécifiques du cerveau par voie transcrânienne (c’est-à-dire à travers la boîte crânienne), sans qu’une intervention chirurgicale invasive soit nécessaire. Ce terme regroupe différentes méthodes utilisant chacune des mécanismes physiques uniques tels que les champs magnétiques , les ondes ultrasonores focalisées, les courants électriques et les ondes de choc acoustiques pour influencer l’activité neuronale.
Quelles sont les procédures NIBS disponibles ?
Parmi les méthodes NIBS les plus connues figurent des procédés tels que la Stimulation Transcrânienne par Impulsions (TPS), la Stimulation Magnétique Transcrânienne (TMS), la Stimulation Magnétique Transcrânienne Répétitive (rTMS), les Ultrasons Focalisés Transcrâniens (tFUS) et la Stimulation Transcrânienne à Courant Continu (tDCS).
Ces procédures se distinguent notamment par leur champ d’application, leur protocole de traitement et le mécanisme physique utilisé pour moduler l’activité neuronale dans le cerveau : La TMS et la rTMS sont basées sur des champs magnétiques pour stimuler le cerveau, les tFUS sont des ondes ultrasonores focalisées pour une stimulation cérébrale profonde et précise, la tDCS utilise des courants électriques pour modifier l’excitabilité neuronale et la TPS utilise des ondes de choc acoustiques pour atteindre des structures cérébrales plus profondes et stimuler les processus neuronaux.
Stimulation Transcrânienne par Impulsions
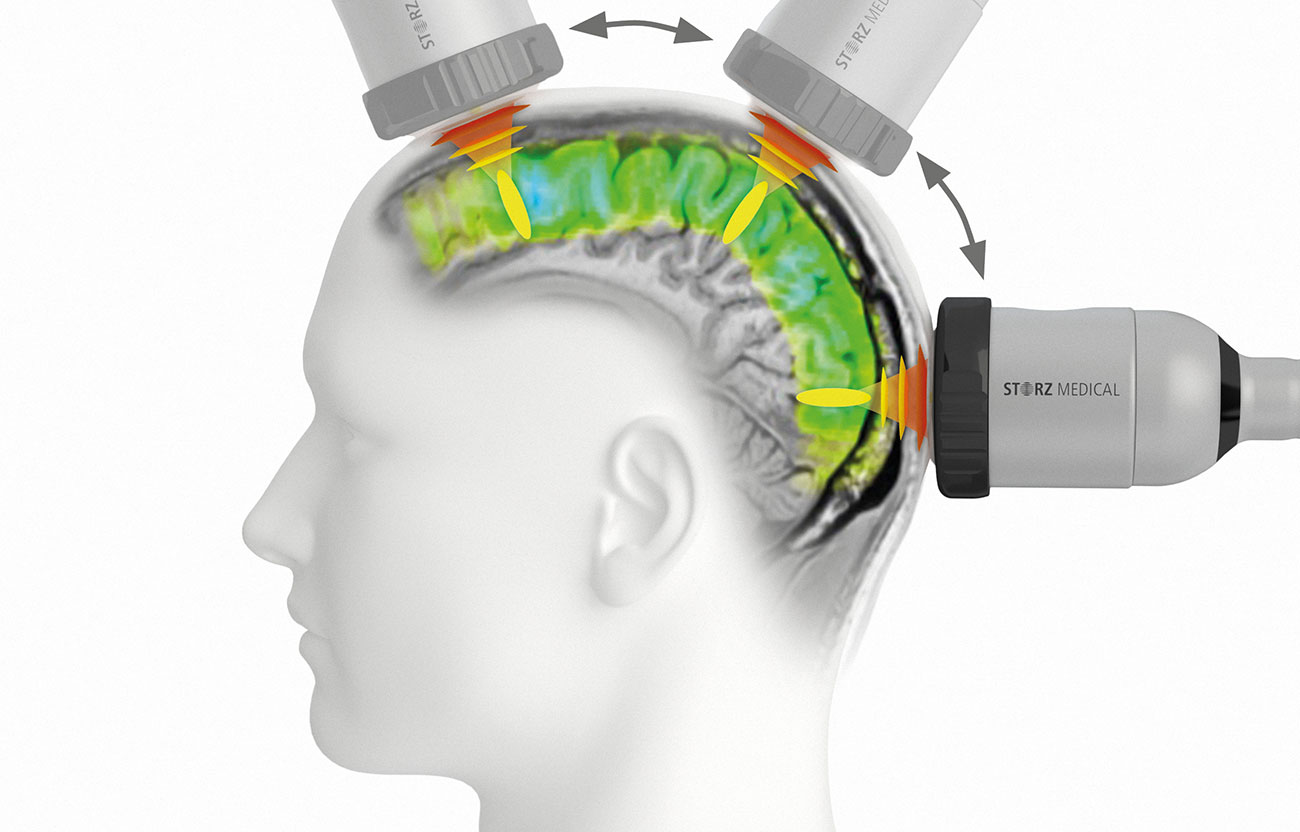
La Stimulation Transcrânienne par Impulsions (TPS) est une méthode qui utilise des ondes de choc (ondes acoustiques pulsées) pour délivrer de l’énergie physique sur des zones tissulaires localisées. Un applicateur placé sur le cuir chevelu génère des ondes pulsées qui délivrent des énergies ciblées dans des régions spécifiques du cerveau. Elles présentent une zone focale en forme d’ellipse allongée de 3 à 6 cm et libèrent des énergies cliniquement efficaces jusqu’à une profondeur de pénétration de 8 cm.
Les avantages sont l’application manuelle et extrêmement contrôlée des impulsions dans les régions ciblées et le protocole de traitement compact, qui consiste en seulement six séances sur une période de deux semaines. Une séance dure généralement 30 minutes et a lieu en ambulatoire. Il n’est pas nécessaire de raser le cuir chevelu.
La TPS avec le système NEUROLITH®, qui a obtenu le marquage CE en 2018, est une option de traitement d’accompagnement pour les patients atteints de la maladie d’Alzheimer.
Des études actuelles indiquent une bonne sécurité[10] et des modifications neuroplastiques[11] et morphologiques[2] possibles grâce à la TPS, ainsi qu’une amélioration des performances et des fonctions cognitives globales chez les patients atteints de la maladie d’Alzheimer[12]. Des études cliniques récentes ont en outre démontré une amélioration significative des symptômes de la dépression chez les patients atteints de la maladie d’Alzheimer[13, 14]. D’autres projets de recherche sont en cours pour clarifier les effets à long terme, les mécanismes d’action et les effets biologiques de la TPS.
Stimulation Magnétique Transcrânienne
La Stimulation Magnétique Transcrânienne et la Stimulation Magnétique Transcrânienne répétitive (respectivement TMS et rTMS) sont des méthodes non invasives utilisées en neurologie et en psychiatrie pour traiter différentes maladies. La Stimulation Magnétique cérébrale consiste à utiliser des champs magnétiques pour stimuler des neurones dans des régions spécifiques du cerveau[1, 2]. Il est ainsi possible d’agir de manière ciblée sur des aires du cerveau et de modifier l’activité neuronale.
Pour ce faire, la TMS génère une courte impulsion magnétique sur le cuir chevelu, qui traverse les tissus jusqu’au cerveau. Cette méthode est utilisée dans la pratique clinique, par exemple pour traiter la dépression, les troubles de la douleur ou certains types de troubles moteurs[3, 4]. En outre, elle est souvent utilisée à des fins de recherche pour étudier le fonctionnement de certaines aires du cerveau. La profondeur de pénétration est généralement de 2 à 3 cm, avec un maximum de 5 cm pour la méthode dite Deep TMS[5][6].
Stimulation Magnétique Transcrânienne répétitive
La stimulation Magnétique Transcrânienne répétitive (rTMS) constitue une extension de la TMS. Il s’agit d’appliquer des impulsions magnétiques répétitives, c’est-à-dire répétées, afin d’influer sur l’activité neuronale sur une période prolongée. L’utilisation répétée sur plusieurs séances sert à induire des changements à long terme dans l’activité et la connectivité neuronales. La rTMS est principalement utilisée dans le traitement des dépressions graves qui ne répondent pas aux thérapies traditionnelles[7]. En outre, des recherches et des études cliniques sont en cours dans d’autres domaines d’application potentiels tels que les troubles anxieux, la schizophrénie et la rééducation après un accident vasculaire cérébral[8].
La TMS et la rTMS interviennent toutes deux de manière ciblée sur l’activité cérébrale, sans qu’il soit nécessaire de recourir à une opération ou à des implants permanents. Elles sont considérées comme sûres et présentent moins de risques d’effets secondaires[2] que les méthodes invasives, bien que l’effet exact ainsi que l’utilisation optimale fassent toujours l’objet de recherches scientifiques[1].
Différents protocoles de traitement sont utilisés en fonction du domaine d’application. Mais en règle générale, les traitements par TMS et rTMS comprennent 20 à 30 séances de 15 à 40 minutes. Les séances ont généralement lieu 5 jours par semaine sur une période de 4 à 6 semaines.
Stimulation Transcrânienne à Courant Continu
La Stimulation Transcrânienne à Courant Continu (tDCS) est une autre technique de stimulation cérébrale non invasive utilisée pour moduler l’activité neuronale. Cette méthode utilise des courants électriques de faible intensité pour moduler l’excitabilité neuronale et la plasticité dans des zones spécifiques du cerveau. La tDCS utilise des paires d’électrodes, chacune composée d’une anode et d’une cathode, placées de manière ciblée sur le cuir chevelu pour faire passer un flux de courant continu de faible intensité à travers des parties spécifiques du cerveau (d’une électrode à l’autre).
Le mode d’action de la tDCS repose sur l’hypothèse que l’application d’un faible courant continu peut modifier les potentiels membranaires de repos des neurones, ce qui entraîne une augmentation ou une diminution de l’activité neuronale. L’anode doit alors augmenter l’activité neuronale sous l’électrode (effet excitateur), tandis que la cathode la diminue (effet inhibiteur)[9].
La tDCS fait l’objet de recherches et est utilisée dans une multitude de domaines d’application, notamment pour améliorer les fonctions cognitives telles que l’apprentissage, la mémoire et la concentration, pour traiter la dépression, pour gérer la douleur et pour soutenir la rééducation après un accident vasculaire cérébral[8]. L’un des avantages particuliers de la tDCS réside dans sa simplicité et sa sécurité, ce qui rend la méthode attrayante pour une utilisation dans des environnements cliniques et de recherche.
Alors que la tDCS a montré des résultats prometteurs dans différentes études, l’efficacité exacte et le mode d’application optimal (comme l’intensité du courant, la durée et le placement des électrodes) font encore l’objet de recherches actuelles dans de nombreux domaines. La réponse individuelle à la tDCS peut varier et il est recommandé de n’utiliser cette technique que sous la supervision ou sur la recommandation d’un professionnel de la santé.
Un protocole de traitement par tDCS typique pour la dépression ou l’amélioration des symptômes cognitifs comprend environ 10 à 20 séances de 20 à 30 minutes chacune, à un rythme quotidien ou quasi quotidien, sur une période de 2 à 4 semaines.
Ultrasons Focalisés Transcrâniens
Les Ultrasons Focalisés Transcrâniens (tFUS) sont une technologie avancée et non invasive qui utilise les ondes ultrasonores pour stimuler de manière ciblée les régions profondes du cerveau. Contrairement aux autres méthodes de stimulation cérébrale, les tFUS permettent une focalisation très précise, de sorte que des zones spécifiques du cerveau peuvent être traitées sans intervention chirurgicale.
Cette méthode consiste à envoyer des ondes ultrasonores concentrées à travers la boîte crânienne, qui se concentrent sur un point précis du cerveau. Ce point d’énergie focalisé peut moduler l’activité neuronale, soit en stimulant les cellules, soit en inhibant leur activité, selon le réglage des ultrasons. L’un des principaux avantages des tFUS est leur capacité d’atteindre des structures cérébrales plus profondes, difficilement accessibles par d’autres méthodes non invasives comme la TMS ou la tDCS.
Les tFUS font l’objet de recherches cliniques pour un certain nombre d’applications potentielles, notamment le traitement de maladies neurologiques et mentales telles que la maladie de Parkinson, la maladie d’Alzheimer, la dépression sévère et la douleur chronique. En outre, des recherches sont en cours sur la possibilité d’utiliser les tFUS pour améliorer les fonctions cognitives ou moduler les états de conscience.
La sécurité et l’efficacité des tFUS continuent de faire l’objet de recherches approfondies, l’objectif étant d’établir cette technologie comme une méthode thérapeutique précise et efficace pour un grand nombre de maladies cérébrales.
La recherche sur les tFUS étant encore en cours, il n’existe pas de protocoles de traitement standardisés. Les premiers résultats suggèrent qu’un traitement pourrait prendre la forme de plusieurs séances étalées sur quelques semaines. La durée des séances peut varier de 30 minutes à plusieurs heures.
NIBS : Une technologie d’avenir ?
Étant donné que les signaux dans le cerveau sont principalement transmis par des impulsions électriques soutenues par des processus chimiques, le fonctionnement du cerveau peut être modulé par différents procédés externes qui génèrent de faibles champs électriques. C’est pourquoi les procédures NIBS constituent une option de traitement prometteuse et douce pour compléter les soins médicaux existants dans les maladies qui touchent principalement le cerveau. Ces procédures peuvent souvent être réalisées en ambulatoire et ne nécessitent pas d’intervention chirurgicale ni l’administration de médicaments supplémentaires. Ils n’ont donc pas d’effet sur les traitements en cours et conviennent parfaitement comme option de traitement d’appoint conviviale pour les patients.
Au cours des 20 dernières années, le nombre d’études sur les NIBS a fortement augmenté[15], ce qui indique que cette technologie est de plus en plus pertinente et qu’elle est bien tolérée dans les maladies neurologiques et psychologiques[16]. Des études récentes s’intéressent de plus près à la question suivante : quelles procédures associées à quels protocoles de traitement, seraient efficaces sur quelles maladies. Bien que des recherches supplémentaires soient nécessaires pour démontrer et délimiter plus précisément l’efficacité de ces procédures, ces techniques prometteuses ont le potentiel d’être utilisées plus largement à l’avenir pour améliorer la qualité de vie des personnes touchées.
Références
1. Jannati, A., et al., Assessing the mechanisms of brain plasticity by transcranial magnetic stimulation. Neuropsychopharmacology, 2023. 48(1): p. 191-208.
2. Rossi, S., et al., Safety and recommendations for TMS use in healthy subjects and patient populations, with updates on training, ethical and regulatory issues: Expert Guidelines. Clin Neurophysiol, 2021. 132(1): p. 269-306.
3. McClintock, S.M., et al., Consensus Recommendations for the Clinical Application of Repetitive Transcranial Magnetic Stimulation (rTMS) in the Treatment of Depression. J Clin Psychiatry, 2018. 79(1).
4. Mutz, J., et al., Comparative efficacy and acceptability of non-surgical brain stimulation for the acute treatment of major depressive episodes in adults: systematic review and network meta-analysis. BMJ, 2019. 364: p. l1079.
5. Samoudi, A.M., et al., Deep Transcranial Magnetic Stimulation: Improved Coil Design and Assessment of the Induced Fields Using MIDA Model. Biomed Res Int, 2018. 2018: p. 7061420.
6. Kedzior, K.K., et al., Deep transcranial magnetic stimulation (DTMS) in the treatment of major depression: An exploratory systematic review and meta-analysis. J Affect Disord, 2015. 187: p. 73-83.
7. Ontario, H., Repetitive Transcranial Magnetic Stimulation for People With Treatment-Resistant Depression: A Health Technology Assessment. Ont Health Technol Assess Ser, 2021. 21(4): p. 1-232.
8. Fregni, F., et al., Evidence-Based Guidelines and Secondary Meta-Analysis for the Use of Transcranial Direct Current Stimulation in Neurological and Psychiatric Disorders. Int J Neuropsychopharmacol, 2021. 24(4): p. 256-313.
9. Nitsche, M.A., et al., [Modulation of cortical excitability by transcranial direct current stimulation]. Nervenarzt, 2002. 73(4): p. 332-5.
10. Beisteiner, R., et al., Transcranial Pulse Stimulation with Ultrasound in Alzheimer's Disease-A New Navigated Focal Brain Therapy. Adv Sci (Weinh), 2020. 7(3): p. 1902583.
11. Chen, X., et al., Transcranial pulse stimulation in Alzheimer's disease. CNS Neurosci Ther, 2024. 30(2): p. e14372.
12. Menardi, A., et al., Toward noninvasive brain stimulation 2.0 in Alzheimer's disease. Ageing Res Rev, 2022. 75: p. 101555.
13. Matt, E., G. Dorl, and R. Beisteiner, Transcranial pulse stimulation (TPS) improves depression in AD patients on state-of-the-art treatment. Alzheimers Dement (N Y), 2022. 8(1): p. e12245.
14. Cheung, T., et al., Evaluating the efficacy and safety of transcranial pulse stimulation on adolescents with attention deficit hyperactivity disorder: Study protocol of a pilot randomized, double-blind, sham-controlled trial. Front Neurol, 2023. 14: p. 1076086.
15. Huang, Y.Z., et al., Plasticity induced by non-invasive transcranial brain stimulation: A position paper. Clin Neurophysiol, 2017. 128(11): p. 2318-2329.
16. Oberman, L.M. and P.G. Enticott, Editorial: The safety and efficacy of noninvasive brain stimulation in development and neurodevelopmental disorders. Front Hum Neurosci, 2015. 9: p. 544



